Die Neuroradiologie wird zur Aufarbeitung der akquirierten Patientinnen bzw. Patienten und Bilddaten zunehmend durch den Einsatz von Artificial Intelligence (AI) und Computer-aided diagnosis (CAD)-Verfahren unterstützt.
Bei der Erforschung und Entwicklung innovativer Applikation aus den Bereichen AI und CAD besteht eine enge Partnerschaft mit klinischen Partnern der Universitätsmedizin Erlangen, dem Lehrstuhl für Mustererkennung und Industriepartnern. In Zusammenarbeit mit dem Lehrstuhl für Mustererkennung evaluieren wir z.B. Möglichkeiten der Bildverbesserung u.a. durch den Einsatz von deep learning.
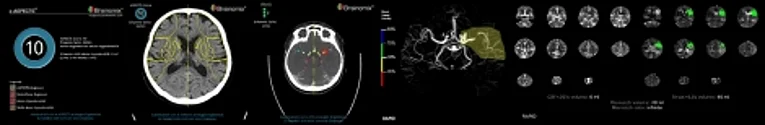
Computer-aided diagnosis in der Schlaganfalldiagnostik
Der Einsatz von CAD kann u.a. bei der Prognoseeinschätzung des akut ischämischen Schlaganfalls helfen. Durch die automatisierte Auswertung des Parenchymschadens, sowie der statischen und dynamischen Gehirndurchblutung, kann so eine patientenindividualisierte Therapie weiter vorangetrieben werden. Dabei ermöglicht AI, bzw. CAD eine quantifizierbare Aufarbeitung der gewonnen Informationen, die die Grundlage für die weitere Behandlungsstrategie bilden.
Zahlreiche Vorarbeiten, enge und gewachsene Kooperationen mit Partnern aus Klinik, Wissenschaft und Industrie, sowie eine umfangreiche Datenbasis ermöglichen uns Impulse zur Verbesserung bestehender Produkte zu geben, als auch maßgeblich an der Gestaltung neuer Applikationen mitzuwirken und eine zügige Translation der Forschungsergebnisse in die klinische Routine zu erzielen.
Dosisersparnis durch Artificial Intelligence
Die 3D-Rotationsangiographie (3D DSA) ist eine essentielle Flachdetektorapplikation zur dreidimensionalen Visualisierung der Hirnarterien. Die 3D DSA hilft zum einen bei der Detektion kleinster Befunde (z.B. winzige Aneurysmata) und zum anderen bei der Analyse komplexer Gefäßerkrankungen. Die 3D DSA ist daher eine der am häufigsten durchgeführten Flachdetektorapplikationen in der interventionellen Neuroradiologie und verursacht konsekutiv auch eine signifikante Strahlendosis. Innovative, auf AI basierende Algorithmen können hier helfen, Gefäßstrukturen dreidimensional ohne Informationsverlust mit deutlich reduzierter Strahlendosis (um bis zu 50%) zu visualisieren. Ziel unserer Forschung ist hierbei v.a. die Validierung und Optimierung dieser AI-basierten Verfahren und eine Überführung unserer Forschungsergebnisse in die klinische Implementierung. Zudem sollen auch weitere Flachdetektor-Applikationen in der interventionellen Neuroradiologie von diesem AI-Algorithmus profitieren.
In der interventionellen Neuroradiologie kann AI helfen Strahlendosis für Patient und Untersucher zu reduzieren. Zusammen mit Siemens Healthineers evaluieren und optimieren wir u.a. AI-Algorithmen, die es ermöglichen dreidimensionale Bilder der Hirngefäße zu erstellen und dabei fast 50% der Dosis einsparen.
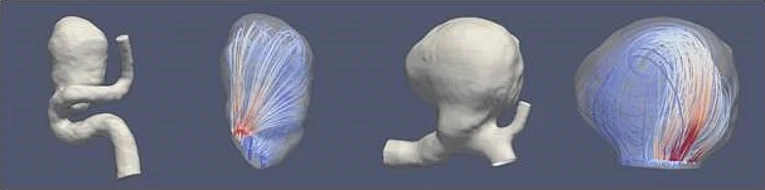
Untersuchungen zur Hämoynamik-Simulation zerebraler Aneurysmen
Die Nutzung von 3D-Daten der Hirngefäße als Grundlage für räumlich und zeitlich aufgelöste Strömungssimulationen ermöglicht es, die hämodynamisch bedingte mechanische Belastung zerebraler Aneurysmen zu quantifizieren. In Kooperation mit dem Lehrstuhl für Mustererkennung und Siemens Healthineers konnte hier ein Prototyp-Algorhithmus zur schnellen Simulation entwickelt werden. Damit sollen die Wirkung verschiedener endovaskulärer Therapiemethoden – insbesondere der Einsatz flussmodulierender Aneurysmastents (Flow Diverter) – an einer Vielzahl von klinischen Fällen im Detail untersucht werden. Auch andere Pathologien (Stenosen, arteriovenöse Malformationen) könnten zukünftig von diesen Entwicklungen profitieren. Mittel- und langfristiges Ziel ist die Entwicklung und klinische Implementierung einer automatisierten Software-Plattform im interventionellen Umfeld.
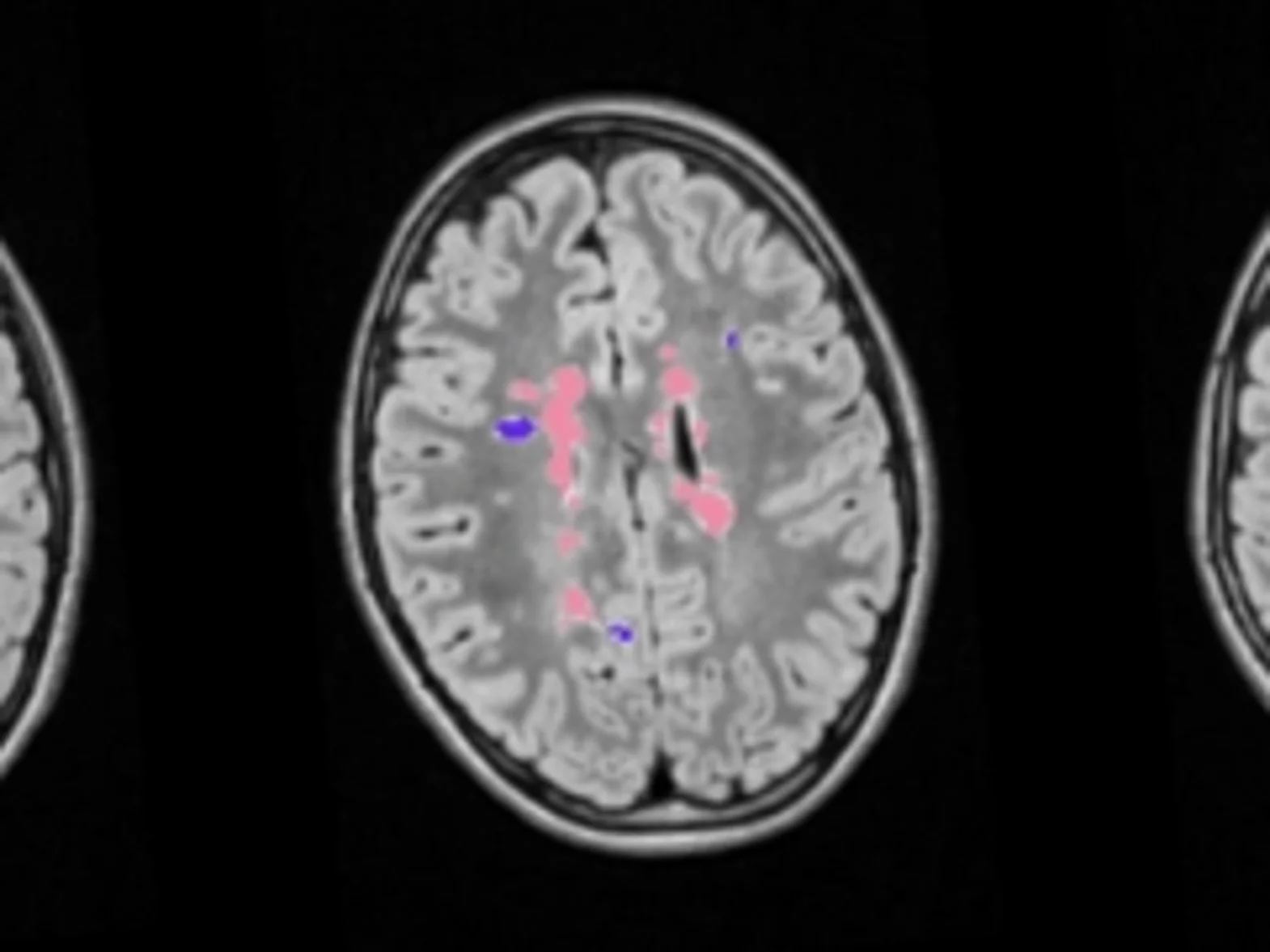
Artificial Intelligence und Neurodegeneration
In Kooperation mit Industriepartnern evaluieren wir den Einsatz von KI bei der Auswertung neurodegenerativer Prozesse, z.B. durch eine automatisierte und quantifizierte Bewertung des Hirnvolumens. Auch die Dynamik entzündlicher Veränderungen lässt sich KI-unterstützt quantifizieren.
Ansprechpartner: Dr. med. Philip Hölter, Dr. med. Stefan Lang
Auswahl Literatur:
Hölter P, Mühlen I, Gölitz P, Beuscher V, Schwab S, Dörfler A. Automated ASPECT scoring in acute ischemic stroke: comparison of three software tools. Neuroradiology. 2020;62:1231-1238.
Lang S, Hölter P, Birkhold AI, Schmidt M, Endres J, Strother C, Dörfler A, Lücking H. Quantitative and Qualitative Comparison of 4D-DSA with 3D-DSA Using Computational Fluid Dynamics Simulations in Cerebral Aneurysms. AJNR Am J Neuroradiol. 2019;40:1505-1510.
Lang S, Hoelter P, Schmidt M, Eisenhut F, Kaethner C, Kowarschik M, Lücking H, Doerfler A. Evaluation of an Artificial Intelligence-Based 3D-Angiography for Visualization of Cerebral Vasculature. Clin Neuroradiol. 2019 Oct 9. doi: 10.1007/s00062-019-00836-7
Stimpel B, Syben C, Würfl T, Breininger K, Hoelter P, Dörfler A, Maier A.Projection-to-Projection Translation for Hybrid X-ray and Magnetic Resonance Imaging. Sci Rep. 2019 Dec 11;9(1):18814. doi: 10.1038/s41598-019-55108-8.
Stimpel B, Syben C, Schirrmacher F, Hoelter P, Doerfler A, Maier A. Multi-Modal Deep Guided Filtering for Comprehensible Medical Image Processing. IEEE Trans Med Imaging. 2019 Nov 22. doi: 10.1109/TMI.2019.295518
Schirrmacher F, Köhler T, Endres J, Lindenberger T, Husvogt L, Fujimoto JG, Hornegger J, Dörfler A, Hoelter P, Maier AK. Temporal and volumetric denoising via quantile sparse image prior. Med Image Anal.2018 Jun 6;48:131-146
Schmidt M.A.,Linker R.A., Lang S., Lücking H., Engelhorn T., Kloska S., Uder M., Cavallaro A., Dörfler A., Dankerl P. (2017) FLAIRfusion Processing with Contrast Inversion Improving Detection and Reading Time of New Cerebral MS Lesions. Clin Neuroradiol. 2017 Mar 6. doi: 10.1007/s00062-017-0567-y.
Boegel M, Hoelter P, Redel T, et al. A fully-automatic locally adaptive thresholding algorithm for blood vessel segmentation in 3D digital subtraction angiography. Conf Proc IEEE Eng Med Biol Soc. 2015;2015:2006-9.
Gölitz P, Lücking H, Hölter P, Knossalla F, Dörfler A. What is the hemodynamic effect of the Woven EndoBridge? An in vivo quantification using time-density curve analysis. Neuroradiology. 2020;62:1043-1050